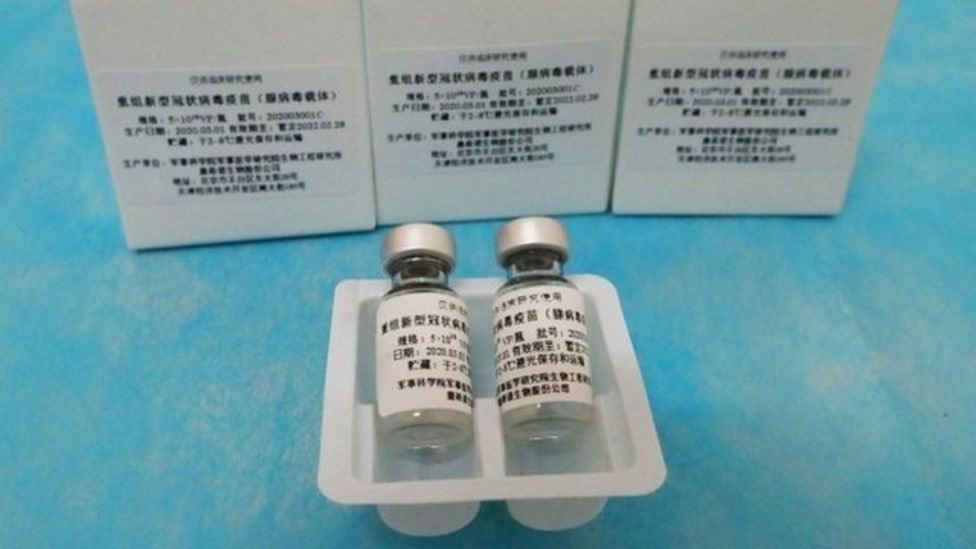
Вакцина Sinovac уже вводится в Китае в рамках программы экстренного использования, но еще не завершила клинические испытания в Бразилии, Турции и Индонезии.
Клинические испытания китайской вакцины против COVID-19 были приостановлены в Бразилии после того, как органы здравоохранения сообщили о «серьезном» неблагоприятном инциденте.
Регулирующий орган Бразилии Anvisa сообщил, что инцидент произошел 29 октября, но не сообщил подробностей.
Вакцина CoronaVac, разработанная китайской компанией Sinovac Biotech, является одной из нескольких, которые во всем мире проходят заключительную фазу тестирования.
Sinovac заявил, что он «уверен в безопасности вакцины».
Фирма уже использовала его для иммунизации тысяч людей в Китае в рамках программы экстренной помощи.
Прекращение испытаний вакцины Sinovac произошло вскоре после того, как немецкая компания Pfizer объявила об отличных результатах испытаний вакцины, которую она разрабатывает вместе с BioNTech.
Почему испытания остановили?
В понедельник Anvisa заявила, что «постановила прервать клинические испытания вакцины CoronaVac после «серьезного неблагоприятного инцидента». Но не раскрыла, что произошло и где это произошло.
Заключительные испытания вакцины Sinovac также продолжаются в Индонезии и Турции, но ни одна из этих стран не объявила о приостановке.
Государственная компания Индонезии Bio Farma заявила во вторник, что ее собственные испытания вакцины Sinovac «проходят гладко», сообщает агентство Reuters.
Димас Ковас, директор Института Бутантана, медицинского исследовательского института, проводящего судебное разбирательство в Бразилии, сказал местным СМИ, что остановка испытаний была связана со смертью.
Однако он также настаивал на том, что смерть не была связана с вакциной, сообщает Reuters.
Со своей стороны, Sinovac заявил во вторник, что поддерживает связь с Бразилией.
«Мы узнали, что директор Института Бутантана считает, что это серьезное побочное явление не связано с вакциной», — говорится в заявлении компании.
«Клиническое исследование в Бразилии проводится строго в соответствии с требованиями GCP (Надлежащая клиническая практика), и мы уверены в безопасности вакцины», — говорится в сообщении.
Пауза в клиническом исследовании не является чем-то необычным. В сентябре Великобритания остановила испытания другой вакцины от COVID-19 после того, как у участника возникло подозрение на побочную реакцию.
Испытания вакцины, разрабатываемой AstraZeneca и Оксфордским университетом, возобновились через несколько дней после того, как регулирующие органы заявили, что продолжение испытаний безопасно.
Президент Бразилии Жаир Болсонару открыто продемонстрировал свое предпочтение вакцине, разрабатываемой AstraZeneca, заявив, что его правительство не будет покупать вакцину китайского производства.
Бразилия была одной из стран, наиболее пострадавших от коронавируса, где было зарегистрировано более 5,6 миллиона подтвержденных случаев, что является третьим по величине показателем в мире после США и Индии.
По данным, собранным Университетом Джонса Хопкинса, на сегодняшний день в южноамериканской стране погибло почти 163 тысячи человек.
Как Китай использовал экспериментальные вакцины?
В дополнение к испытаниям третьей фазы, проходящим за рубежом, Китай также вводит экспериментальные вакцины против COVID-19 внутри страны.
CoronaVac — одна из трех экспериментальных вакцин против коронавируса, которые Китай использует для вакцинации сотен тысяч людей в рамках программы экстренного использования.
Сотни людей выстроились в очереди, чтобы получить вакцину, после того как власти одобрили ее распространение среди всех, кто хотел сделать инъекцию. Sinovac ранее заявлял, что вакцину получили почти все ее сотрудники и их семьи.
Представитель китайского здравоохранения ранее сказал, что в ходе клинических испытаний не было замечено серьезных побочных эффектов.